硝酸是一种无机化合物,化学式为HNO3。它是一种强腐蚀性的无机酸。该化合物是无色的,但由于分解成氮氧化物,较旧的样品往往呈黄色。大多数市面上销售的硝酸在60-98%之间。其中中国60%稀硝酸为主,浓硝酸一般在98%(占大多数)。美国的稀硝酸浓度为68%稀硝酸为主,更浓的硝酸在86%。
因为有二氧化氮分解,呈现出烟雾状态,通常呈现出红色烟雾,当硝酸浓度达到95%以上时,烟雾颜色变成白色。

硝酸的主要化学性质
硝酸具有强氧化性和酸性、一般可以发生:酸碱中和反应、与金属发生反应(根据浓度不同,可生成氢气、一氧化氮和二氧化氮),与非金属发生反应(生产一氧化氮、二氧化氮),黄蛋白实验(与蛋白质反应生成黄色消化物,添加氨等碱性物质后,变成橙色),当然硝酸也可以在加热的条件下发生分解反应,生成一氧化氮和二氧化氮。

硝酸的生产
工业化生产:商业级硝酸溶液通常含有 52% 至 68% 的硝酸。硝酸的生产是通过以德国化学家Wilhelm Ostwald的名字命名的奥斯特瓦尔德法进行的。在此过程中,在约 500 K(227 °C;440 °F)的高温和 9 个标准大气压(910 kPa)的压力下 ,在铂或铑丝网催化剂存在下,无水氨被氧化成一氧化氮。
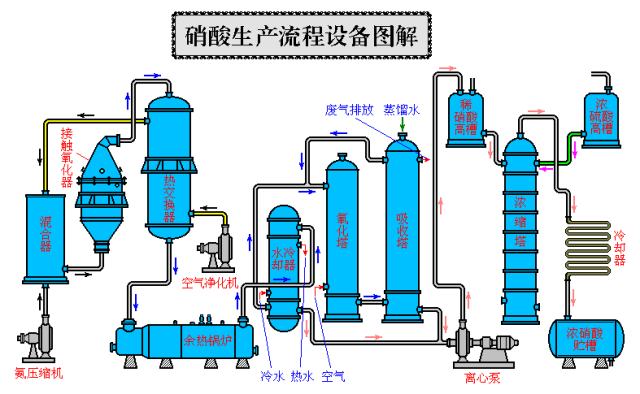
硝酸的应用
❖有机工业:用于制造四硝基甲烷、硝基己烷、l-硝基丙烷、2,4-二硝基苯氧乙醇等硝基化合物。
❖染料工业:用于对硝基苯甲醚、4,4’-二硝基二苯醚、对硝基苯酚、2,5-二氯硝基苯等染料中间体的合成。
❖涂料工业:用于制造硝基清漆和硝基瓷漆。
❖医药工业:用于制造硝基苯乙酮。
❖水处理:可用作碳素钢、不锈钢设备的清洗除锈剂,用在污水、废水的氧化还原处理过程中。在污水的生物法处理过程中,可用作微生物养分中的氮源等。
急救措施
皮肤接触:立即脱去污染的衣着,用大量流动清水冲洗20~30分钟。如有不适感,就医。
眼睛接触:立即提起眼睑,用大量流动清水或生理盐水彻底冲洗10~15分钟。如有不适感,就医。
吸入:迅速脱离现场至空气新鲜处。保持呼吸道通畅。如呼吸困难,给输氧。呼吸、心跳停止,立即进行心肺复苏术。就医。
本文共分 1 页



